胶质母细胞瘤(GBM)是成人最常见且恶性程度最高的原发性脑肿瘤,患者中位生存期不足20个月,预后极差。目前,标准治疗方案包括手术切除、替莫唑胺化疗及放疗。其中,放疗是延长患者生存期最有效的一线治疗手段。然而,几乎所有患者最终都会因放疗抵抗而复发死亡,这与肿瘤内存在一类具有自我更新和放疗抵抗能力的“胶质母细胞瘤干细胞(GSCs)”密切相关。如何打破这种放疗抵抗,成为改善患者预后的关键难题。
近日,生物医学创新研究院/基础医学院张泽延研究员与纽约大学、杜克大学等机构合作,在《Nature Communications》期刊上发表了题为“NANP targeting radiosensitizes glioblastoma through TNFR1 sialylation-driven mesenchymal shift”的研究论文,首次揭示了唾液酸合成通路关键酶NANP通过调控肿瘤坏死因子受体1(TNFR1)唾液酸化修饰及内吞,激活NF-kB通路并驱动GSCs向间质(MES)表型转化,成为放射增敏的潜在靶点。

该研究以患者来源的GSCs为模型,首先利用单细胞DNA条形码谱系追踪技术发现,放疗抵抗与靶向治疗耐受不同,并不显著富集特异性耐受亚克隆,提示“全局放射增敏”是更可行的策略。团队进一步通过全基因组CRISPR筛选,研究识别出唾液酸合成通路关键酶NANP是排名靠前的未知放射增敏靶点,且其高表达与肿瘤放疗抵抗密切相关。实验表明,靶向沉默NANP可显著增强放射诱导的肿瘤细胞DNA损伤、G2/M期阻滞及凋亡,从而提升GBM对放疗的敏感性。机制研究发现,NANP通过调控TNFR1的唾液酸化修饰及内吞,激活NF-κB信号通路,驱动GSCs向MES表型转化,最终导致肿瘤放疗抵抗。
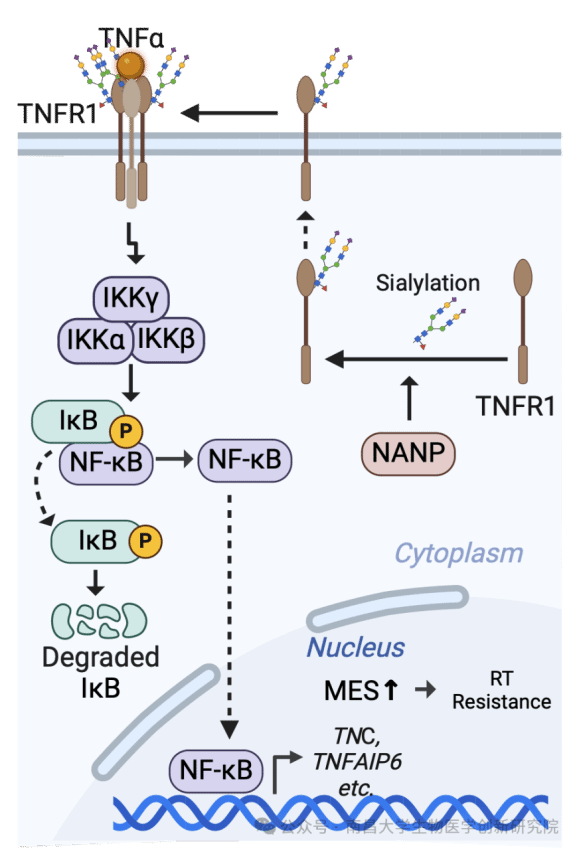
该研究揭示了胶质母细胞瘤放疗抵抗的形成机制,也为开发新型放疗增敏剂提供了重要的理论依据和潜在靶点。
生物医学创新研究院/基础医学院张泽延研究员与丁颖雯博士为该论文共同第一作者,杜克大学癌症研究所代理执行所长/放射肿瘤学系主任Erik P. Sulman教授为通讯作者。南昌大学为第一单位。
原文链接:https://www.nature.com/articles/s41467-026-70853-x
(来源:南昌大学生物医学创新研究院微信公众号)

